|
مروری بر وضعیت تب های بازگرد در ایران؛ دکتر احسان مصطفوی
تعريف بيماري
تب بازگرد (Relapsing fever) جزء بيماريهاي عفوني حاد است كه توسط بند پاياني از قبيل كنه ها و شپش منتقل مي شود و از نظر باليني با حملات عود كننده تب و اسپيروكتمي مشخص ميگردد، تابلوي باليني بيماري شامل حملا ت تب و لرز است كه بر خلاف مالاریا دارای دوره های چند روزه تب و فاقد تب ميباشد. در تب بازگرد هر مرحله تب دار آن 2 تا 9 روز و معمولا 6-5 روز است و چند روز متوقف (6-2 روز) و دوباره شروع مي شود. دفعات عود معمولاً 10-1 بار خواهد بود و بدون درمان، بهبودي از بيماري تا 40 روز طول خواهد كشيد.
شپش تن انسان ناقل بورليا رکورنتیس است كه سبب تب بازگرد شپشي و يا اپيدميك مي شود و كنه هاي جنس اورنيتودوروس انتقال دهنده انواع زيادي از گونه هاي بورليا هستند كه موجب تب بازگرد كنه اي يا اندميك مي شوند.
عامل بيماري
عامل بيماري نوعي باكتري از جنس بورليا است كه در خارج گلبول های قرمز خون يافت نمي شود، اين ارگانيسم باريك و كشيده به شكل مارپيج، قابل انعطاف، متحرك، فاقد زوائد لرزان و غشاي مواج است. بورلياهاي منتقله توسط كنه مي توانند براي مدت 15 سال در بدن ناقل طبيعي خود زنده بمانند و اين روش مناسب براي حفظ ارگانيسم ها است. با توجه به اختصاصي بودن ناقل براي هر نوع از بورليا، از اين روش جهت تشخيص گونه آنها استفاده مي شود.
مخازن بيماري
الف) تب بازگرد اپيدميك: انسان تنها مخزن شناخته شده در تب بازگرد اپيدميك مي باشد.
ب) تب بازگرد اندميك: جوندگاني نظير سنجاب، خرگوش و موش هاي صحر ايي به دليل اينكه بورلیاها مي توانند به مدت طولاني در جريان خون آنها باقي بمانند به عنوان مخزن اصلی بيماري شناخته مي شوند .کنه های ماده آلوده به دليل اينكه بورليا را مستقيماً از راه تخم به نسل بعدی منتقل میکنند نيز در زمره مخازن قرار مي گيرند.
راه انتقال بيماري
اين بيماري داراي ناقل بوده و انتقال مستقيم از شخص به شخص ندارد.
الف) نوع اپيدميك: توسط بورليا ركورانتيس ايجاد مي شود و به وسيله شپش تن انسان (پديكولوزيس هومانوس) از فردي به فرد ديگر منتقل مي گردد. پس از آنكه شپش، خون آلوده انسان را هضم كرد، اسپيروكت ها در ديواره لوله گوارش نفوذ و در همولنف تكثير پيدا مي كنند. بافت هاي بدن شپش مورد تهاجم اسپيروكت ها قرار نمي گيرد و به همين دليل اين بيماري از طريق بزاق يا مواد دفعي شپش به انسان يا از راه تخم به نسل بعدي بندپا منتقل نمي شود. با توجه به اين مسئله، تب بازگرد اپيدميك در اثر له کردن شپش در روي بدن است كه باعث آزاد شدن ارگانيسم هاي آلوده كننده مي شود كه قدرت نفوذ در پوست يا پوشش مخاطي سالم را دارند. شپش ها براي تمام مدت عمر خود (10 تا 60 روز) آلوده كننده باقي مي مانند و انسان تنها ميزبان اين ارگانيسم است. وقوع اپيدمي هاي بيماري تب بازگرد شپشي اغلب با شرايط و حوادث غير مترقبه نظير جنگ، قحطي، زلزله، سيل و ... كه سبب ازدحام زياد جمعيت در اردوگاه ها و پخش شپش تن مي گردند همراه است. اين آلودگي در حال حاضر كانون هاي محدودي در آسيا، آفريقاي شرقي (بورندي، اتيوپي و سودان) مناطق مرتفع آفريقاي مركزي و آمريكاي جنوبي دارد.
ب) نوع اندميك: کنه های نرم می توانند در تمام مراحل چرخه حیاتی (نوزاد، نمف و بالغین) از طریق خونخواري عامل بيماري را از طريق بزاق يا مواد دفعی، منتقل نمايند. عامل بيماري مستقيما از انسان به انسان منتقل نمی شود. انتقال آلودگي از طريق تخم به نسل بعدي كنه، يك راه مهم بقاي آلودگي است و كنه هاي آلوده مي توانند به مدت 2 تا 15 سال بدون تغذيه زنده بمانند.
انتشار بيماري
تب بازگرد كنه اي به غير از مناطق محدودي از جنوب غربي اقيانوس کبیر در تمام دنيا مشاهده مي شود؛ وقوع تب بازگرد اپیدمیک بيشتر بستگي به عوامل اقتصادي و اجتماعي دارد، اما در مورد تب بازگرد اندميك وقوع بيماري بيشتر به بيولوژي كنه ناقل و شرايط جغرافيائي وابسته است.
به طور كلي بروز و برقراري تب بازگرد به عواملی چون وجود افراد حساس و فاقد ايمني، وجود كنه نرم يا شپش تن آلوده به بورليا، تماس انسان با كنه يا شپش آلوده، توانايي ناقل نسبت به انتقال عامل بيماري، وجود مخزن عامل بيماري در منطقه و انتقال بورليا به نسل بعد توسط كنه ها بستگی دارد.
پراکنش بیماری در دنیا
فرم های اصلی بیماری شامل:
1-تب بازگرد منتقله بوسیله کنه که بوسیله کنه های نرم جنس Ornithodoros ایجاد می شود و بیشتر در آفریقا، اسپانیا، عربستان، آسیا و نواحی مشخصی از غرب آمریکا مشاهده می شود. گونه هایی از باکتری که در بروز تب بازگرد دخیل هستند شامل Borrelia duttoni ، B.hermsii ، parkerii B. می باشند.
2-تب بازگرد منتقله توسط شپش بدن که بیشتر در آسیا، آفریقا و مرکز و جنوب آمریکا رخ می دهد و عامل آن recurrentis B. می باشد.
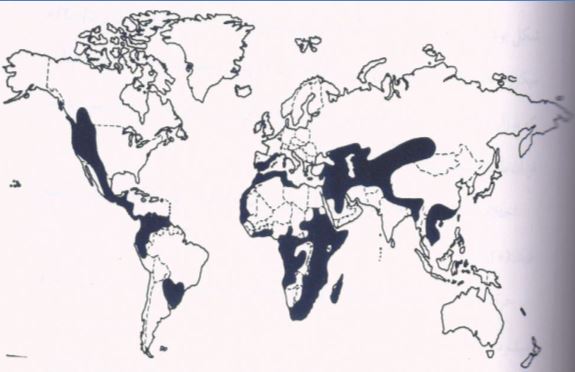
انتشار جغرافیایی تب بازگرد در دنیا(1)
تاريخچه و وضعیت بيماري در ايران
بورلیا پرسیکا برای اولین بار از خون یک بیمار اردبیلی توسط ووشن کوفسکی و لاس در سال 1291 جدا شده است(2). از سال 1316 مطالعات گسترده اي در ایران جهت شناخت بيولوژي، اكولوژي و اپيدميولوژي بورلياها و ناقلين آنها توسط انستيتو رازي شروع و در سالهای بعد با پيگيري محققين انستیتو پاستور ايران آقايان دكتر شمس الدين مفيدي، دكتر محمود بهمنيار، دكتر بيوك سيديان و دکتر منصور شمسا با راهنمايي هاي پروفسور مارسل بالتازار همراه شده و با تجسسات علمي اساتید بخش انگل شناسي دانشكده پزشكي تهران آقايان دكتر انصاري و دكتر جهانبخش ادامه يافته و ثمرات بسيار ارزنده اي در محافل علمي جهان به بار آورد. آقاي دكتر عزيز رفيعي ساليان سال تحقيقات ارزنده اي درباره عامل و ناقل تبهاي بازگرد كنه اي در ايران نموده و در سال 1325 موفق به كشف بورلياي جديدي در ايران به نام بورليا ميكروتي در مناطق جنوبي ايران شد(3). طي سال هاي بعد حضور بورلياي لاتيشوي كه در سال 1941 توسط Sofievمعرفي شده بود نيز در ناحيه شمال ايران به كمك كارشناسان انستيتو پاستور ایران محقق گرديد.
در سال 1355 آقاي دكتر يونس کریمی، نمونه بورليايي را از بيماري جدا نمود که پس از بررسی های ساختمان آن با ميكروسكوپ الكتروني مشخص گرديدكه با ساير گونه ها متفاوت است و به نام B. Baltazardi نامگذاري گرديد(4). لذا تاكنون گونه هاي بورليا پرسيكا، بورليا ميكروتي، بورليا لا تشوي و بورليا بالتازاردي در كنه هاي ايران يافت شده است و بورليا پرسيكا و بورليا بالتازاردي را فراوان از خون بیماران مبتلا به تب بازگرد کنه ای جدا نموده اند و طبق گزارش دكتر كريمي در سال 1355 حدود 38 درصد بيماران تب دار روستاي كورائيم از توابع استان اردبيل مبتلا به اين بيماري بوده اند.
همه گيري تب بازگرد شپشي يك بار در سال های 9- 1298 در شرق ايرا ن، نواحي بيرجند و مشهد و تربت حيدريه را فرا گرفته و بار ديگر در سال های 5- 1322 تهران، آبادان و در چندين نقطه ديگر كشور وقوع داشته است.
در سال 1360، مرحوم دکتر یونس کریمی حاصل نتایج مطالعات صورت گرفته روی تب های بازگرد را در کتابی با نام مشابه منتشر نمود(5).

در طول سالیان اخیر با تدوين و اجراي برنامه های مختلف پيشگيري و مبارزه با بيمار و تربيت و به كارگيري نيروي انساني متخصص در نظام سلامت كشور به ويژه در مناطق اندميك و ارتقاء ارائه خدمات بهداشتی و آموزشي و مراقبتي و همچنين به علت صرف اعتبارهاي وسیع و كلان در بخش بهداشت و بهسازي مناطق مسكوني انساني و محل هاي نگهداري دامها، شاهد كاهش شديد آمار مبتلايان و كنترل بيماري بوديم به طوري كه ميزان آلودگي از بيش از 38% در بيماران تب دار در مناطق روستاي اردبيل در سال 1355، به 2/11 درصد بيماران تب دار در سال 1365 در این استان رسیده است. 46 درصد موارد بیماری در سال 1365 در اردبیل در نوزادان و كودكان قبل از دبستان، رخ داده است و عامل بيماري (بورليا پرسيكا) علاوه بر انسان از 18ـ12 درصد كنه هاي اورنيتودوروس تولوزاني آن منطقه يافته شده است(6).
در سال هاي 1372ـ1371 در شهرستان زنجان، نمونه هاي خوني تهيه شده، پس از مشاهدات ميكروسكوپي مستقيم و بررسي سرولوژيكي ايمونوفلورسانس غير مستقيم (IFA) ، آلودگي به بورليا و عيار آنتي بادي بورليا پرسيكا رديابي گرديده و مشخص شده است كه 24 نفر از هر ده هزار نفر افراد مورد مطالعه دچار آلودگي به بورليا در خون محيطي، بوده اند. همچنين در بررسي سرولوژيكي نمونه ها مشخص شده كه در 3/5% افراد جامعه مورد بررسي، آنتي بادي بورليا پرسيكا با عيار 1:80 در گروه هاي مختلف سني و جنسي ساكنين اين مناطق، مثبت بوده است.
در مطالعه ای که در سال 1386 و 1387 در قزوین انجام شد، 7/16 درصد کنه های Ornithodoros tholozani آلوده به بورلیا پرسیکا بودند(7).
اين بيماري در ايران از ساليان قديم مورد توجه بوده و برنامه هاي مختلف مبارزه و مطالعاتي در مورد آن صورت گرفته، به طوريکه تاکنون بيش ترين بررسي ها بر روي بيماري در دنيا از ايران گزارش شده است با توجه به اهميت زياد بيماري، از سال 1379 نظام مراقبت بيماري توسط مرکز مديريت بيماري ها طراحي و در کشور به اجرا گذاشته شده که طي اين برنامه ضمن ارايه آموزش به جامعه و پرسنل فني نظام سلامت، از تمامي افراد تب دار و مشکوک، گستره خون محيطي تهيه و از نظر آلودگي به بورليا مورد بررسي قرار مي گيرد.
با توجه به اقدامات همه جانبه بين بخشي و درون بخشي و پيگيريهاي مستمر و برنامه هاي عملياتي متعدد تدوين و اجرا شده، عملاً گزارش بيماري بسیار کم شده است به طوری که تعداد موارد بیماری به 17 مورد در كل جمعیت كشور (0.02 در يكصد هزار نفر) در سال 1389 رسيده و در سال 1390 در مجموع تنها 13 مورد بيماري از استان هاي همدان، كردستان، قزوين، سمنان، هرمزگان گزارش شده است(1). با این وجود به نظر می رسد قسمتی از کاهش موارد ممکن است ناشی از عدم گزارش موارد بیماری یا عدم توجه پزشکان به این بیماری باشد.
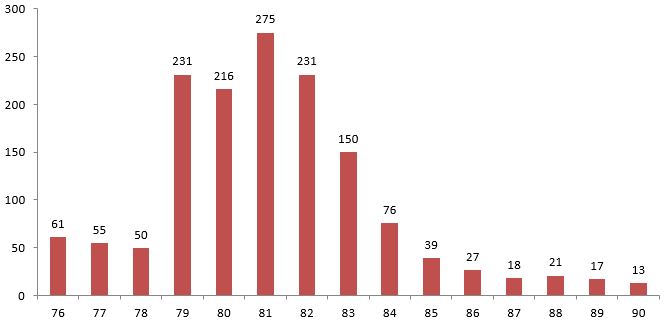
روند گزارش موارد بيماري تب بازگرد در ايران از سال 1376 تا 1390
به علت زئونوتيك بودن تب بازگرد کنه ای و احتمال وقوع اپيدمي هاي تبهاي بازگرد شپشي در اثر بوجود آمدن بحران هاي مختلف، لازم است تا نظام بهداشتي بيش از پيش نسبت به اجرا دقیق برنامه هاي مراقبتي و انجام پایش بیماری در مخازن و ناقلین بیماری بويژه در مناطق اندميك كوشا باشد.
بورلياهاي عامل تب بازگرد در ايران
الف) تب بازگرد شپشي يا همه گير: توسط بورليا ركورانتيس ايجاد مي شود و به وسيله شپش تن انسان از فردي به فرد ديگر منتقل مي گردد.
ب) تب بازگرد كنه اي يا اندميك: نوع کنه ای بیماری در ایران بیشتر شایع است.
از مجموع 36 گونه بورلياي شناسايي شده در سطح جهان، 17 گونه به عنوان عامل تب بازگرد شناخته شده اند؛ تاكنون چهارگونه بورليا در ايران مورد شناسائي قرار گرفته است كه عبارتند از بورليا پرسيكا (B. Persica)، بورليا ميكروتي (B.microti)، بورليا لاتيشوي (B. latyschewii) و بورليا بالتازاردي ((B. baltazardi.
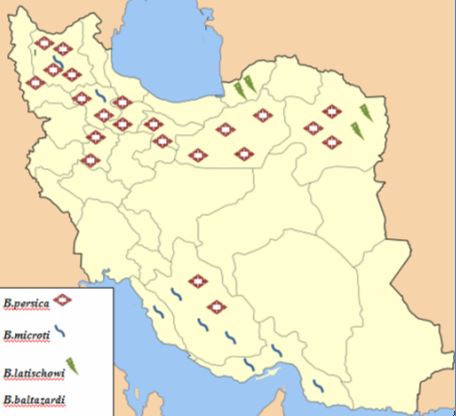
پراكندگي گونه هاي بورليا در ايران(1)
ناقلين تب بازگرد اندميك در ایران
انواعي از كنه هاي نرم جنس اورنيتودوروس (Ornithodoros) از خانواده آرگازيده ناقلين اصلي اين بيماري مي باشند. 3 گونه از این کنه ها که در ایران شناسایی شده شامل اورنیتودوروس تولوزانی (ناقل بورلیا پرسیکا)، اورنیتودوروس اراتیکوس (ناقل بورلیا میکروتی) و اورنیتودوروس تارتاکوفسکی (ناقل بورلیا لاتیشوی) هستند.
انواعي از كنه هاي نرم جنس اورنيتودوروس (Ornithodoros) از خانواده آرگازيده ناقلين اصلي اين بيماري مي باشند. 3 گونه از این کنه ها که در ایران شناسایی شده شامل اورنیتودوروس تولوزانی (ناقل بورلیا پرسیکا)، اورنیتودوروس اراتیکوس (ناقل بورلیا میکروتی) و اورنیتودوروس تارتاکوفسکی (ناقل بورلیا لاتیشوی) هستند.
1- اورنيتودوروس تولوزاني (:(Ornithodoros tholozani اين کنه در سال 1313 براي اولين بار در ایران شناسايي شد و ناقل اصلي تب بازگرد در كشور محسوب مي شود. در مناطق كوهستاني غرب، شمال و شمال غرب اردبیل، آذربايجان شرقي و غربي، زنجان، گيلان، مازندران، همدان، قزوين، دماوند، فيروزكوه، سمنان، سبزوار، نیشابور، اصفهان و دامنه هاي جنوبي زاگرس انتشار دارد. مناطقي نظير ميانه، زنجان و شاهرود به عنوان كانون هاي تب بازگرد كنه اي، شناخته شده اند.
2- اورنيتودوروس اراتيكوس ( :(Ornithodoros erraticusاين كنه در استان هاي خوزستان، هرمزگان، سيستان و بلوچستان، بوشهر، اصفهان، ساوه، قزوين، كرج، سمنان، پارس آباد مغان و آذربايجان غربي، انتشار دارد.
3- اورنيتودوروس تارتاكوفسكي (:(Ornithodoros Tartakovski اين كنه در شمال شرقي كشور در استان هاي خراسان، سرخس، گنبد و تركمن صحرا انتشار دارد.
اين كنه ها در محل خنك و تاريك نظير دالان هاي لانه جوندگان، شكاف ديوارهاي اصطبل ها (پناهگاه حيوانات) و غارها و درون چوب هاي پوسيده زندگي مي كنند و مي توانند سال ها بدون تغذيه زنده باقي بمانند. کنه ها ترجيحاً از خون جوندگان تغذيه می کنند اما ممكن است در مواقعي كه ميزبان اصلي در دسترس نباشد از پستانداران ديگري نظير انسان تغذیه نمایند.
کنههای نرم معمولاً در طول شب و ظرف مدت 5 تا 30 دقيقه خونخواري می كنند، گزش آن ها بدون درد است و به همين دليل است كه بيشتر مردمي كه مورد تهاجم كنه قرار می گیرند گزش آن را به ياد نمی آورند.
براي بورليا بالتازاردي تاكنون ناقل طبيعي در ايران شناسايي نشده است.

پراكندگي ناقلين تب بازگرد در ايران(1)
پراکندگی بیماری در ایران
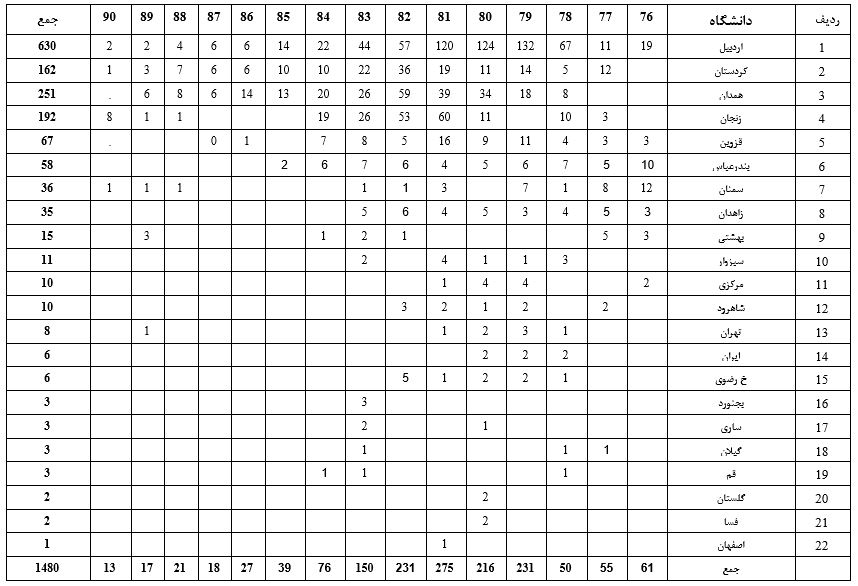
تب بازگرد يكي از مشكلات مهم بهداشتي اغلب استان هاي كشور بويژه مناطق روستائي است و تاکنون موارد بيماري از 21 استان کشور گزارش شده است.
وضعيت بيماري تب بازگرد در ايران از سال 1376 تا 1390 (1)
رفرانس ها
1. محرم مافي، سعيدرضا نداف، حسين معصومي اصل، سيد محسن زهرايي، راهنماي كشوري مراقبت بيماري تبهاي راجعه 1392، وزارت بهداشت، درمان و آموزش پزشکی، 56 صفحه.
2. Delpy L, Rafyi A. Sur la fievre recurrente sporadique en Iran. Contribution a l'etude experimentale de Spirochaeta persica Dschunkowsky, 1913. Ann Parasitol Hum Comp1939. 1939;17:45-61.
3. Rafyi A. Sur la fievre recurrente sporadique en Iran. Etude experimentale de Spirochaeta persica (deuxime note) Archives de l Institut d'Hessarek1946.2:37-42.
4. Karimi Y, Hovind-Hougen K, Birch-Andersen A, Asmar M, editors. Borrelia persica and B. baltazardi sp. nov.: experimental pathogenicity for some animals and comparison of the ultrastructure. Annales de microbiologie; 1978.
5. Karimi Y. Recurrent fever and its epidemiology Tehran. Iran: Pasteur Institute of Iran Publications. 1980:55-8.
6. Arshi S, Majidpour A, SADEGHI H, Emdadi D, Asmar M, Derakhshan M. Relapsing fever in Ardabil, a northwestern province of Iran. 2002;5(3):141-5.
7. Barmaki A, Rafinejad J, Vatandoost H, Telmadarraiy Z, Mohtarami F, Leghaei S, et al. Study on presence of Borrelia persica in soft ticks in Western Iran. Iranian journal of arthropod-borne diseases. 2010;4(2):19.
8. Stanek G, Strle F. Lyme borreliosis. The Lancet. 2003;362(9396):1639-47.
9. Borchers AT, Keen CL, Huntley AC, Gershwin ME. Lyme disease: A rigorous review of diagnostic criteria and treatment. Journal of autoimmunity. 2015;57:82-115.
10. Mostafavi E HA, Khakifirouz S, Chinikar S. Spatial analysis of Crimean Congo hemorrhagic fever in Iran. Am J Trop Med Hyg. 2013;89(6):1135-41.
11. Parola P, Raoult D. Ticks and tickborne bacterial diseases in humans: an emerging infectious threat. Clinical infectious diseases. 2001;32(6):897-928.
12. Adabi M, RAHMANI FA, Ghasemi M. Report of a case of Lyme disease in Mazandaran. 2004.
13. Siadati PTA. A case of Lyme disease (Lyme Borreliosis). Acta Medica Iranica. 2006;44(3):222-4.
14. Vahedi-Noori N, Rahbari S, Bokaei S. The Seasonal Activity of Ixodes ricinus Tick in Amol, Mazandaran Province, Northern Iran. Journal of Arthropod-Borne Diseases. 2012;6(2):129.
15. Hanifeh M, Malmasi A, Virtala A, Nikbakht-Brujeni G, Zahraei Salehi T, Rahbari S. Seroprevalence, geographic distribution and risk factor analysis of Borrelia burgdorferi sensu lato in naturally exposed dogs of Iran. Afr J Microbiol Res. 2012;6:5353-61.
16. Erdem H, Akova M. Leading infectious diseases problems in Turkey. Clinical Microbiology and Infection. 2012;18(11):1056-67.
17. Wilske B. Diagnosis of Lyme borreliosis in Europe. Vector-Borne and Zoonotic Diseases. 2003;3(4):215-27.
18. Naddaf SR, Kishdehi M, Siavashi M. Comparison of PCR-based diagnosis with centrifuged-based enrichment method for detection of borrelia persica in animal blood samples. Iranian journal of arthropod-borne diseases. 2011;5(1):7.
19. Naddaf SR, Ghazinezhad B, Bahramali G, Cutler SJ. Phylogenetic analysis of the spirochete Borrelia microti, a potential agent of relapsing fever in Iran. Journal of clinical microbiology. 2012;50(9):2873-6.
20. Naddaf SR, Ghazinezhad B, Sedaghat MM, Asl HM, Cutler SJ. Tickborne Relapsing Fever in Southern Iran, 2011–2013. Wkly Epidemiol Rec. 2014;89:389-400.
21. Shirani D, Rakhshanpoor A, Cutler SJ, Ghazinezhad B, Naddaf SR. A Case of Canine Borreliosis in Iran Caused by Borrelia persica. Ticks and tick-borne diseases. 2016.
برگشت به بالای صفحه
|